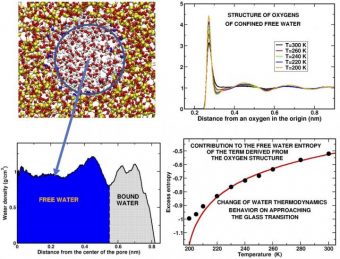
Crediti: Margherita De Marzio, Gaia Camisasca, Maria Martin Conde, Mauro Rovere e Paola Gallo.
L’acqua, lo sappiamo, è il primo ingrediente della vita sul nostro pianeta. La natura è dominata dalla presenza di questo elemento, che in forma di ruscelli, fiumi, mari e oceani, ricopre la gran parte della Terra. Il nostro stesso corpo è fatto per la stragrande maggioranza da acqua. Una molecola famigliare, irrinunciabile e che pur tuttavia nasconde misteri che la scienza non è ancora stata in grado di sciogliere.
Come lo strano fenomeno conosciuto in fisica con il termine “sottoraffreddata”, una sconcertante attività delle molecole d’acqua che mantiene l’elemento allo stato liquido anche al di sotto del normale punto di congelamento.
«Sappiamo bene cosa succede quando l’acqua liquida viene raffreddata al di sotto del suo punto di congelamento: si verifica un cambio di stato e le molecole di dispongono nella struttura cristallina che comunemente chiamiamo ghiaccio», spiega a Media Inaf Paola Gallo, docente di fisica di Roma Tre e fra i firmatari dell’articolo appena pubblicato sul Journal of Chemical Physics. «Tutto cambia però quando sottoponiamo l’acqua a un processo di raffreddamento quasi istantaneo. In questo caso le molecole conservano le caratteristiche tipiche dello stato liquido anche al di sotto del punto di congelamento. L’acqua possiede molte anomalie rispetto agli altri liquidi e varie di queste si acuiscono nel regime sottoraffreddato e sembrano indicare la possibile esistenza di un punto critico liquido-liquido ancora non misurato sperimentalmente. Ma sottoraffreddare l’acqua in laboratorio fino a raggiungere la zona dove il punto critico potrebbe trovarsi è stato finora impossibile».
Grazie alle simulazioni a computer, i ricercatori italiani sono stati in grado di comprendere meglio come le molecole d’acqua ultra-fredde si comportino nelle interazioni fra loro stesse e con le molecole di altri materiali. In passato, gli scienziati hanno cercato di affrontare questo problema lavorando su acqua confinata in griglie porose del raggio di pochi namometri (gli studi nel confinamento sono motivati sia dal loro interesse applicativo che dal fatto che il confinamento consente di raggiungere temperature più basse di sottoraffreddamento). Una condizione di laboratorio tanto estrema da mettere in dubbio però la bontà dell’esperimento. Laddove le molecole d’acqua interagiscono liberamente in grandi volumi, si verificherebbero gli stessi risultati?
«Questa domanda è il punto di partenza del nostro lavoro», spiega Gallo. «In studi precedenti abbiamo già dimostrato come le interazioni con gli altri composti chimici interessino solo le molecole d’acqua prossime alle sostanze esterne. L’acqua che si muove liberamente conserva proprietà inalterate».
La nuova simulazione mostra come partendo dalle proprietà della struttura a rete delle molecole d’acqua è possibile dedurre le variazioni dell’entropia del liquido e rivelare alcune delle stramberie termodinamiche nell’attività dell’acqua in sottoraffreddamento.
Un risultato che crea un quadro di riferimento per gli altri fisici sperimentali, che ora possono ricreare la simulazione con campioni fisici in un laboratorio.
Inutile sottolineare come tutte le informazioni offerte da questo tipo di ricerche possano contribuire a migliorare la nostra conoscenza della “molecola della vita” non solo da un mero punto di vista fisico, ma biologico e chimico che apre a nuove possibilità in ambito tecnologico.
Per saperne di più:
- Leggi su Journal of Chemical Physics l’articolo “Structural properties and fragile to strong transition in confined water” di Margherita De Marzio, Gaia Camisasca, Maria Martin Conde, Mauro Rovere e Paola Gallo




